Steril
Was genau ist eigentlich steril?
Die Sterilität hat in vielen Reinräumen eine wichtige Bedeutung. Als steril wird ein Material, ein Gegenstand, eine Flüssigkeit, eine Oberfläche oder eine bestimmte Umgebung bezeichnet, wenn die Menge aller Mikroorganismen sowie Viren, Bakterien, Prionen und Plasmiden abgetötet oder der überlebende Rest unter einem bestimmten Grenzwert liegt. In der Praxis gelingt eine vollständige Sterilisation in der Regel nicht mit 100%iger Sicherheit.
Inhaltsverzeichnis
- Anwendungsbeispiel
- Verwendung
- Einzelnachweise
- Auswahl steriler Produkte auf pure11
1. Anwendungsbeispiel
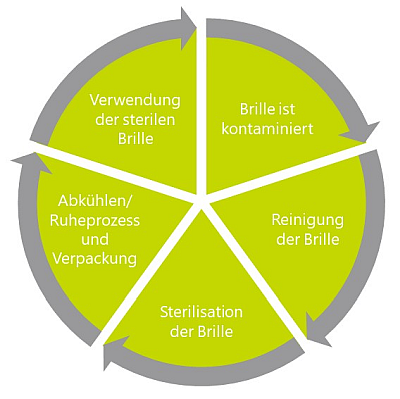
Durch verschiedene Sterilisationsverfahren wie das Autoklavieren, die Gamma-Bestrahlung, die Sterilfiltration oder die Begasung mit Ethylenoxid wird dieser nahezu keimfreie Zustand erreicht und Bakterien effizient abgetötet. Diese Verfahren werden häufig bei der Herstellung und Aufbereitung von Reinraumprodukte eingesetzt.
Abbildung 1: Sterilisation am Beispiel einer Reinraumbrille anschaulich erklärt
2. Verwendung
Typische Branchen, in denen diese Techniken verwendet werden, sind neben allen Bereichen der Medizin auch Bereiche der Biologie und der Pharmazie.
Bei der Herstellung von Arzneimitteln oder Wirkstoffen ist die sterile Arbeit von extrem hoher Bedeutung, um eine Kontamination der Produkte zu verhindern. Besonders bei Arzneimitteln und Medizinprodukten, die direkt in den Körper oder die Blutlaufbahn injiziert werden, ist eine Keimfreiheit anzustreben, damit der Mensch nicht krank wird.
Die Verwendung von sterilen Materialien ist zudem in diesen Risikobereichen gesetzlich vorgeschrieben:
„Das Ziel einer Herstellung unter aseptischen Bedingungen ist, die Sterilität einer aus sterilisierten Bestandteilen zusammengesetzter Zubereitung zu bewahren. Das bedeutet, dass die für die Herstellung notwendigen Ausgangstoffe, einschließlich Primärpackmittel, vor der aseptischen Weiterverarbeitung sterilisiert werden sollten, sofern dies möglich ist, und während der Herstellung keine Kontamination erfolgen darf.“ (Ph.Eur.6 Grundwerk 2008 Teil 5.1.1)
Im Annex 1 des EU-GMP Leitfadens sind detaillierte Leitlinien zur Herstellung steriler Arzneimittel beschrieben. Mit dem neuen Entwurf vom Februar 2020 gelten neue Anforderungen. Was genau sich geändert hat können Sie hier nachlesen.
3. Einzelnachweise
- GMP-Berater: Herstellung unter aseptischen Bedingungen - Maas & Peither AG