Die Reinigungsvalidierung

Verunreinigungen und Kreuzkontaminationen
Partikuläre und mikrobiologische Kontaminationsquellen in Reinräumen können massive Gefahren für die dort herzustellenden Produkte darstellen. Besonders in der pharmazeutischen Industrie, der Herstellung von Arzneimitteln, Medizinprodukten und Medikamenten müssen diese Gefahren auf ein Minimum reduziert werden, was durch eine umfassende Reinigung und Desinfektion erzielt wird. Nur durch eine ausreichende Reinigungsvalidierung kann ein sicheres Produkt gewährleistet werden, welches für den Konsumenten bzw. den Patienten unbeschadet verwendet werden kann.
Im Speziellen fokussieren sich die möglichen Kontaminationsquellen in Reinräumen, die bei einer Validierung berücksichtigt werden müssen, auf Folgende:
- Rohstoffe/ Ausgangsstoffe
- Packmittel
- Reinigungs- und Desinfektionsmittel
- Hilfsmittel, wie Schmierstoffe, Gase oder Werkzeuge
- Umgebungsluft
- Anlagen und Prozessparameter
Eine gut durchdachte Reinraumplanung, besonders hinsichtlich des Hygienic Designs, ist elementar. Lesen Sie in unserem Blog zum Thema „Hygiene im Reinraum“ mehr über die Umsetzung in der Industrie verschiedener Branchen.
Die Grundsätze einer Reinigungsvalidierung
Effektive Reinigungsverfahren sind in verschiedenen Regelungen nach EHEDG (European Hygienic Engineering and Design Group) sowie durch die Regelwerke nach GMP gefordert. Im Allgemeinen sollten Reinigungsverfahren die Eigenschaften von Produkt- und Reinigungsrückständen, den Einfluss der Reinigung auf den Produktionsprozess und seiner Umgebung berücksichtigen und die Anlagen reinigen. Allen voran steht ein hygienisch einwandfreies Design aller produktberührenden Teile.
Um ein gleichbleibendes Ergebnis für eine entsprechend gleichbleibende Produktqualität zu gewährleisten werden die Verfahren der Reinigung validiert und Daten schriftlich festgehalten. Eine Validierung sagt aus, ob ein Prozess oder ein System die vorher gestellten Anforderungen erfüllt. Durch den dokumentierten Nachweis leistet die Reinigungsvalidierung folgende Beiträge:
- Sicherheit des hergestellten Produktes
- Sicherheit des in der Produktion tätigen Personals
- Sicherheit der Umwelt
Im Zuge einer Reinigungsvalidierung wird beispielsweise eine Risikoanalyse verfasst sowie Rückstandsgrenzwerte und Ablaufschemen der Reinigung und Desinfektion schriftlich dokumentiert. Auch werden Reinigungs- und Desinfektionsmittel speziell für die jeweiligen Anlagen und Räume hinsichtlich ihrer Eignung geprüft.
Die Verfahren nach Annex 15
Zwar ist seit der Neufassung des Annex 15 des EU-GMP-Leitfadens das visuelle Kriterium als alleiniges Kriterium einer durchgeführten Reinigung nicht mehr zulässig, dennoch wird das Verfahren als grundlegende Überprüfung einer Reinigung miteinbezogen.
Dabei wird beispielsweise darauf geachtet, dass keine Verkrustungen mehr an den Rohrwandungen kleben und keine sichtbaren Partikel auf den gereinigten Oberflächen sind. Auch werden häufig UV-Lampen eingesetzt, um beispielsweise zurückgebliebene Proteine aufzufinden.
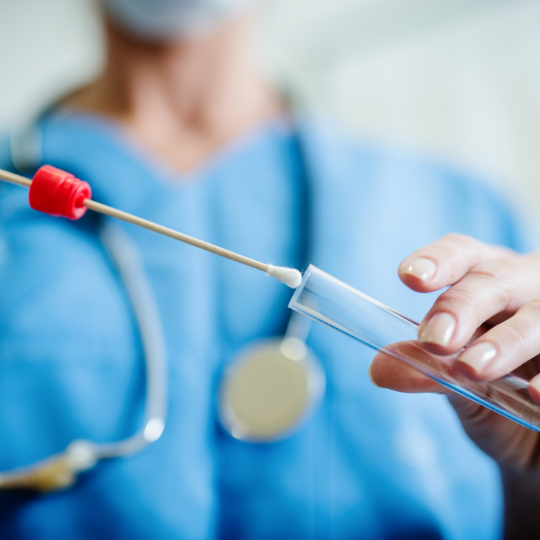
Neben der visuellen Sauberkeit (visually clean) muss mindestens ein weiterer Nachweis der Sauberkeit stattfinden. Meist wird dazu eine Probenentnahme mittels Reinigungsstäbchen, sogenannten „Swabs“, durchgeführt.
Eine definierte Größe einer gereinigten Oberfläche wird mit einem angefeuchteten Probenentnahmematerial abgestrichen. Vorzugsweise erfolgt die Probenentnahme an kritischen Stellen der Produktausrüstung. Diese mechanische Probenentnahme hat den Vorteil, dass auch potentielle Rückstände schwer löslicher Substanzen aufgenommen werden können.
Weitere Maßnahmen zur Erhebung von Daten sind im Zuge der Reinigungsvalidierung zu treffen. Häufig wird eine ATP (Adenosintriphosphat) -Bestimmung durchgeführt. Zusätzlich dazu werden für Abklatschtests RODAC-Platten verwendet, um eine Detektion mikrobieller Verunreinigungen der gereinigten, produktberührenden Oberflächen zu gewährleisten. Beide Verfahren erzielen einen Nachweis von Hefen und Bakterien.
Rahmenbedingungen
Eine zielgerichtete und umfangreiche Reinigungsvalidierung umfasst eine Risikoanalyse. Um eine möglichst hohe Reproduzierbarkeit des Reinigungsverfahren sicherstellen zu können, müssen Art, Menge und Quelle möglicher Kontaminationen bekannt sein und bewertet werden. Je genauer die Erstellung der Validierung erfolgt und je umfangreicher die Ausarbeitung der gewonnen Daten ist, umso konstanter sind die Reinigungsergebnisse später. Aus diesem Grund werden die Arbeitsschritte in einer SOP (Standard Operating Procedure) festgehalten.
Auch Änderungen der Ausrüstung, das heißt des Reinigungsmittels, des Anlagendesigns oder der Prozessumgebung können den Reinigungserfolg beeinflussen, was besonders bei einer häufig wechselnden Produktpalette eine Herausforderung darstellt. In diesem Fall ist es wichtig, auf zuverlässige Informationen der Hersteller zurückgreifen zu können. pure11 informiert nicht nur bei Produktänderungen, sondern hilft auch bei Fragestellungen hinsichtlich der Kompatibilität verschiedener Reinigungsmittel, möglicher Korrosionen und was hinsichtlich der persönlichen Schutzausrüstung zu beachten ist. Selbstverständlich stellen wir Ihnen alle benötigten Daten hinsichtlich des Equipments zur Verfügung.
Das ideale Equipment
Das Abstreichen der gereinigten Flächen mittels Reinigungsstäbchen ist ein Kernelement jeder Reinigungsvalidierung und gehört zu den periodisch durchgeführten Maßnahmen. Sie dient der Dokumentation einer durchgeführten Reinigung. Wie häufig eine Probennahme durchgeführt wird, ist innerhalb einer Risikoanalyse und individuell festzulegen.
Die Analytik des TOC (total organic carbon) -Gehalts ist eine sehr empfindliche Methode. Die Methode dient hauptsächlich der Quantifizierung von Reinigungsmittelrückständen, aber auch von Rückständen biopharmazeutischer Hilfs- und Wirkstoffe, Abbau- und Reaktionsprodukten, mikrobiologischen Rückständen in wässrigen Proben sowie Proteinen und Enzymen.
Um zuverlässige und korrekte Ergebnisse zu erhalten, sollten alle kohlenstoffhaltigen Verbindungen aus der Umgebung entfernt werden. Hinsichtlich der Ausrüstung werden folgende Kriterien empfohlen:
- Der Wischkopf sollte aus Polyester bestehen.
- Der Kunststoffstiel sollte eine Sollbruchstelle enthalten.
- Der Wischkopf sollte mit Reinstwasser angefeuchtet werden.
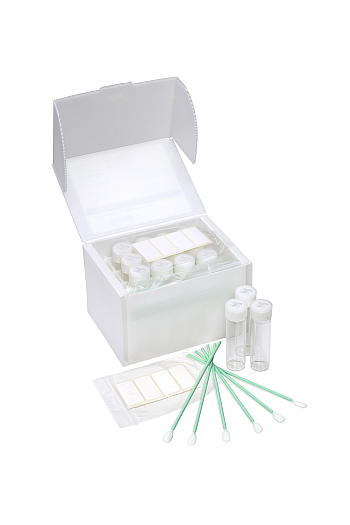
- Das Stäbchen wird nach der Probenaufnahme an der Sollbruchstelle abgeknickt und in einer zugehörigen Probenflasche aufbewahrt und ins Labor zur Analyse transportiert.
Das Kopfmaterial der Stäbchen enthalten TOC-Werte, die mittels sogenannten „Blindproben“ bestimmt werden müssen. Um diesen Schritt während der Analytik zu reduzieren und um zuverlässige und korrekte Ergebnisse zu erhalten, bietet der Hersteller Texwipe speziell für die Reinigungsvalidierung Probenentnahme-Sets an. Die Sets ermöglichen einen effektiven Transport der Proben von der Produktion zum Labor unter Berücksichtigung einer minimalen Kontaminationsgefahr. So enthalten diese Sets Swabs und Lösungen, deren Materialien auf den TOC-Gehalt getestet sind und der vergleichsweise gering ausfällt. Zusätzlich weisen alle Stäbchen eine Sollbruchstelle auf, um den Transport des Stäbchens in einem dafür vorgesehen Probengläschen zu ermöglichen. Ein TOC-Gehalt der Swabs von < 50 µg/L sowie ein TOC-Gehalt der Vials von < 10 µg/L werden vom Hersteller garantiert.
Sie möchten kein gesamtes Kit, sondern nur einzelne Swabs, die auf ihren TOC-Gehalt getestet sind? Hier finden Sie den Tupfer Large Alpha Swab - TX714K und hier den Tupfer Alpha Swab Long Handle - TX761K. Beide Swabs sind aus 100 % Polyester und hinsichtlich ihrer ultra geringen TOC - Gehälter zertifiziert
(< 50 µg/L, < 50 ppb). Weitere Produkte empfehlen wir Ihnen gerne bei einem persönlichen Gespräch. Rufen Sie uns unter der Telefonnummer +49 89 5589434 0 gerne an oder nehmen Sie Kontakt auf!