Qualifizierung
Was ist das?
Eine Qualifizierung ist eine Eignungsprüfung, welche nach verschiedenen Regelwerken gefordert wird und beschreibt die einzelnen Sollwerte zu den Prüfkriterien. Eine erfolgreich abgeschlossene Qualifizierung dient als Beweis, dass ein Produkt, eine Anlage oder Gerätschaft, eine Aktivität, ein Dienstleister, Prozess, Unternehmen oder auch eine Kombination derer in der Lage ist, die Anforderungen zu erfüllen und die darin erwarteten Ergebnisse zu liefern.
Inhaltsverzeichnis
- Anwendungsbeispiel
- Verwendung
- Einzelnachweis
- Auswahl Produkte auf pure11
1. Anwendungsbeispiel
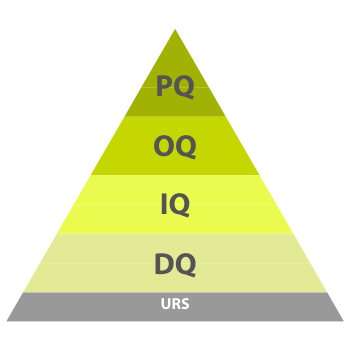
Im Reinraum werden bei der Qualifizierung primär Räumlichkeiten und deren Einrichtungen wie Geräte und Anlagen betrachtet. Die Qualifizierung stellt einen Teil der Qualitätssicherungsmaßnahmen dar, die zu GMP gehören. Kernelement sind Akzeptanzkriterien, wie Grenzwerte oder Spezifikationen. Die Qualifizierung ist in der Pharmabranche die Voraussetzung dafür, dass überhaupt produziert werden darf. Innerhalb einer Qualifizierung wird somit überprüft, ob sich ein Gerät oder Anlage für den vorgesehenen Zweck eignet. Dabei unterteilt sich die Qualifizierung in vier Phasen:
- Designqualifizierung (DQ)
- Installationsqualifizierung (IQ)
- Funktionsqualifizierung (OQ)
- Leistungsqualifizierung (PQ)
Jede Qualifizierungsebene darf erst mit dem Abschluss und damit der Genehmigung der vorherigen Phase beginnen. Nach Beendigung aller vier Qualifizierungsphasen wird vor der abschließenden Freigabe ein Qualifizierungsabschlussbericht erstellt, welcher die gesamte Qualifizierung, deren Ablauf und Ergebnisse dokumentarisch festhält. Mit der Fertigstellung dieses Dokuments erfolgt auch die Freigabe der zu qualifizierenden Einheit. Auch nach der Freigabe und Inbetriebnahme der Räumlichkeiten samt Anlagen gilt, regelmäßig Requalifizierungen, durchzuführen.
2. Verwendung
Um eine Qualifizierung erfolgreich durchführen zu können, bedarf es vorab das Definieren der Anforderungen. Der Annex 15 des EU GMP Leitfadens erfordert das Erstellen einer Benutzeranforderung (URS, User Requirement Specification), aus welcher die Reihe von Anforderungen ausgehen, welche es bedarf, sodass die Technik den vorhergesehenen Zweck erfüllt.
Das Ziel der Qualifizierung ist immer, dass Qualitätsansprüche und alle behördlichen Anforderungen sicher erfüllt werden. Auch wird eine ausreichende Dokumentation der Nachweise gefordert. Qualifizierungen müssen immer nachvollziehbar und reproduzierbar sein.
Dementsprechend müssen Qualifizierungen grundsätzlich geplant und strukturiert erfolgen. Zu erstellende Schlüsseldokumente sind dabei Risikoanalysen, Qualifizierungspläne, Qualifizierungs- und Abweichungsberichte sowie einen Abschlussbericht. Außerdem sollten Requalifizierungen je nach Risikoabschätzung/ -analyse periodisch erstellt und durchgeführt werden. Die Erstqualifizierung wird im Rahmen der Reinraumqualifizierung durchgeführt, wobei die verschiedenen Parameter mittels Monitoring-Systemen überprüft werden.
Dicht angelehnt an die Qualifizierung, und oft mit dieser gemeinsam einhergehend, ist die Validierung.
3. Einzelnachweis
- Buch: GMP-Inspektionen und -Audits (2010)
4. Auswahl Produkte auf pure11
Qualifizierungen werden von Dienstleistern oder entsprechend geschultem Personal durchgeführt. Wir führen keine Qualifizierungen durch, führen aber geeignete Instrumente fürs Monitoring an:
- Partikelzähler
- Partikel-Visualisierungs-Lampe zum Sichtbarmachen fluoreszierender Partikel
Bei Fragen kontaktieren Sie uns jederzeit, wir beraten Sie gerne!